董念国:慢性心衰及终末期心脏病2023年进展
时间: 2024-05-27
作者: 小编:
阅读量: 210
关键词:
华中科技大学同济医学院附属协和医院
董念国教授

本文特邀作者
华中科技大学同济医学院附属协和医院 刘名 王怡轩 董念国
心力衰竭是目前心血管疾病领域唯一呈增长趋势的疾病,随着我国经济的不断增长以及人口老龄化的加重,我国心血管病现患病人数约3.3亿,其中心衰约有890万人。研究显示,心力衰竭5年死亡率达50%,严重者1年死亡率高达50%,心力衰竭已经成为威胁人类健康的重要原因之一。自 1967 年世界首例心脏移植成功实施以来,经过五十余年发展,心脏移植成为目前终末期心力衰竭最有效的治疗手段。但供心短缺严重制约心脏移植发展,全球每年完成心脏移植仅6000 例左右,无法满足持续增长的终末期心力衰竭救治需求。机械循环辅助(MCS)经过50余年发展,技术日趋成熟,可部分或者完全替代心脏功能,已成为心力衰竭患者的有效治疗手段。
短期机械循环辅助(tMCS)
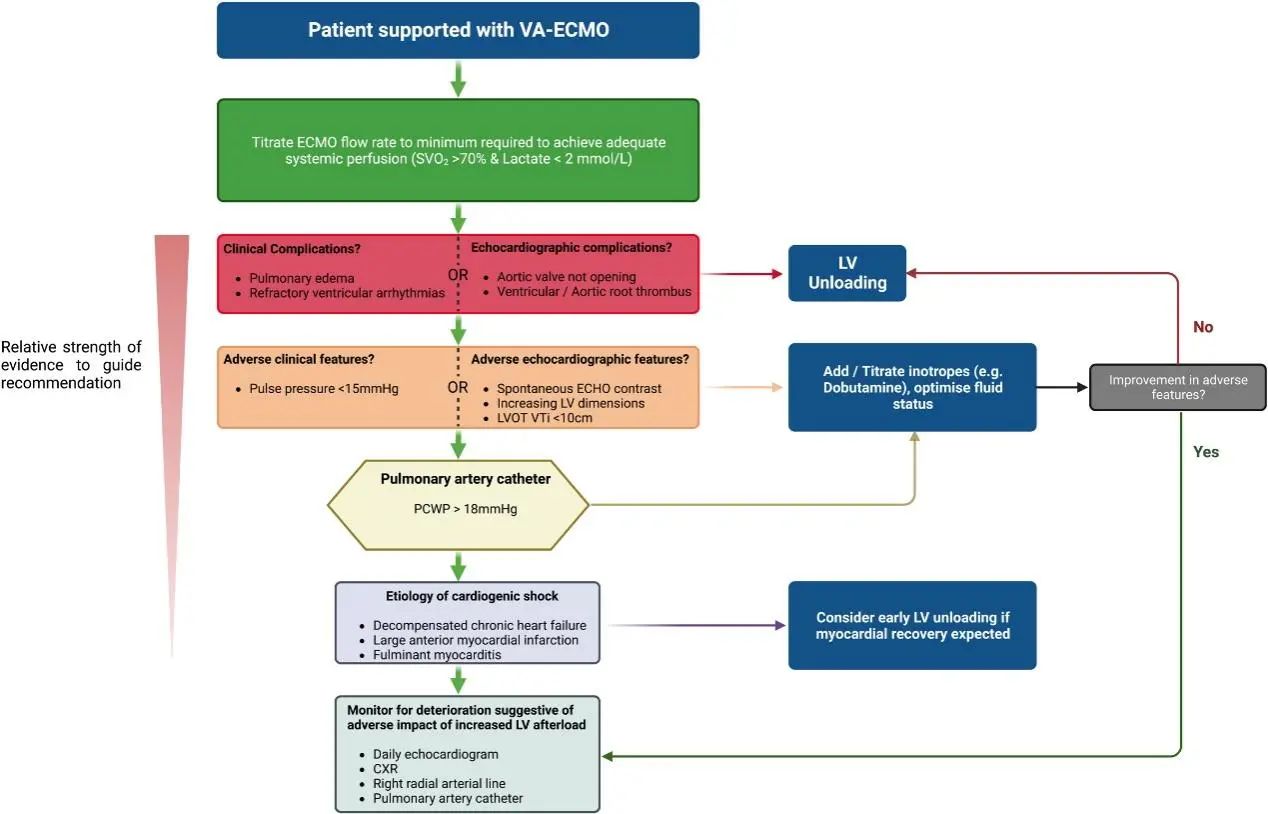
短期机械循环辅助(tMCS)是治疗严重或难治性心源性休克的重要手段之一,tMCS能快速改善全身关键脏器灌注,提供有效循环支持,为患者提供从数小时到数周的血流动力学支持和器官灌注,是病情恢复或临床决策(移植或长期机械循环辅助)的桥梁。过去十年,全球范围内tMCS使用量迅速增加,已成为心衰治疗领域的重要技术。
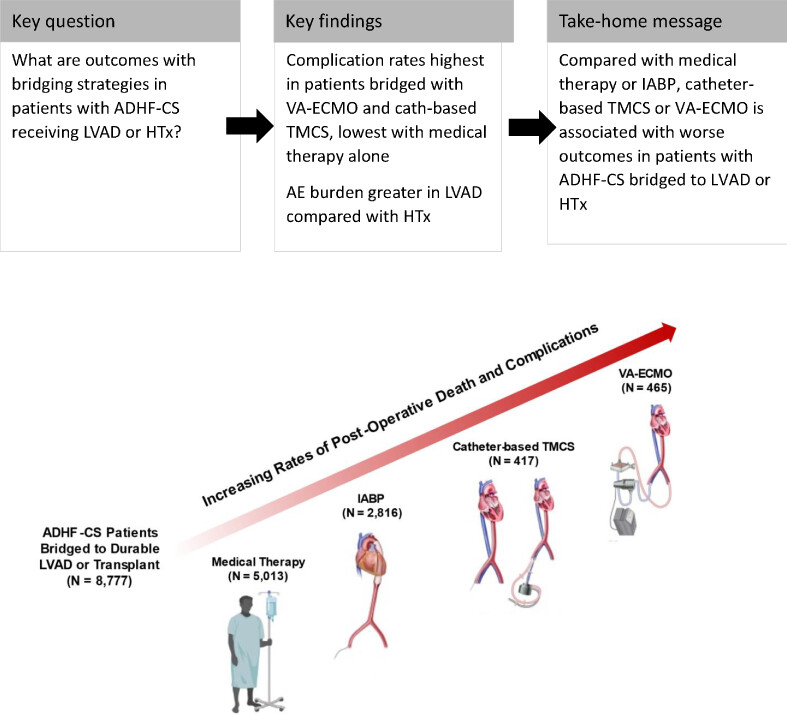
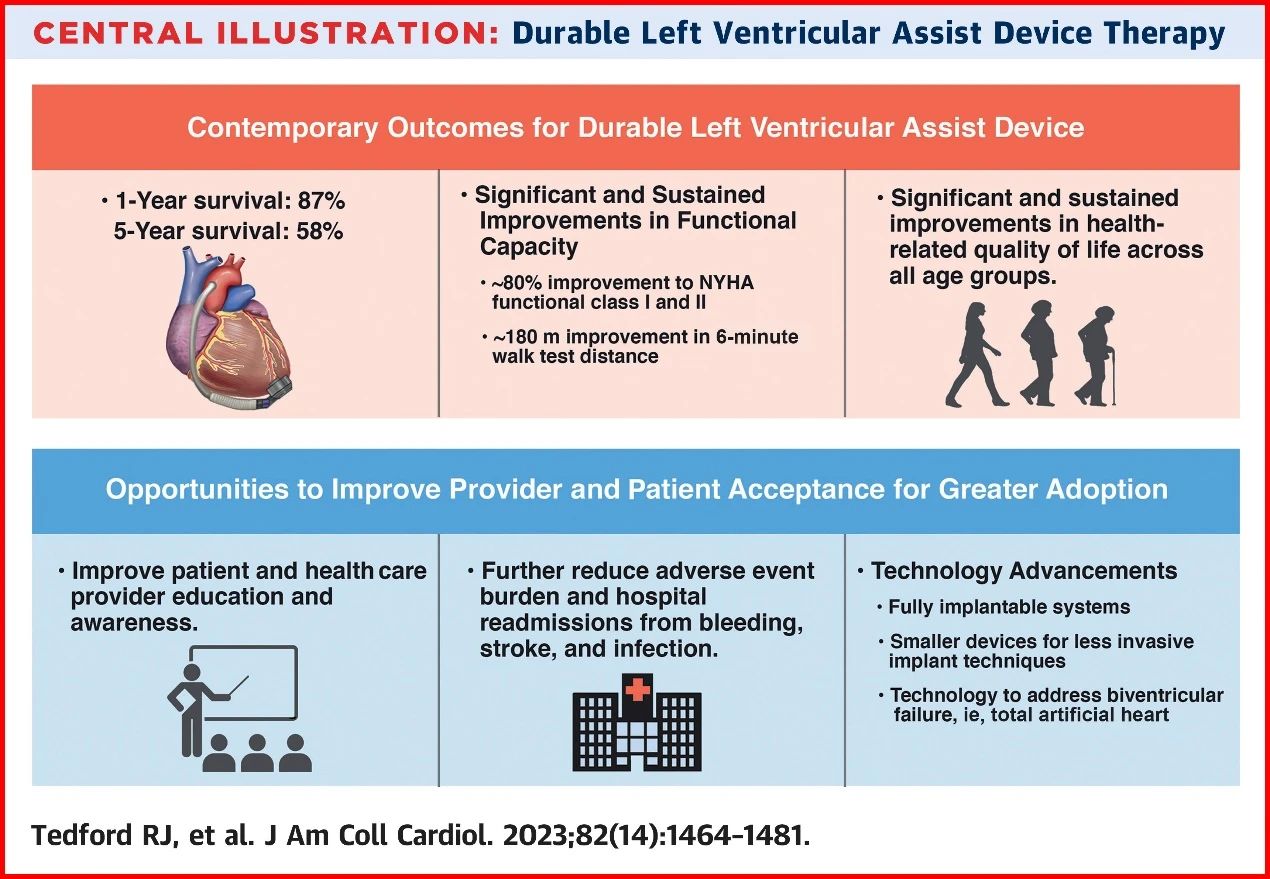
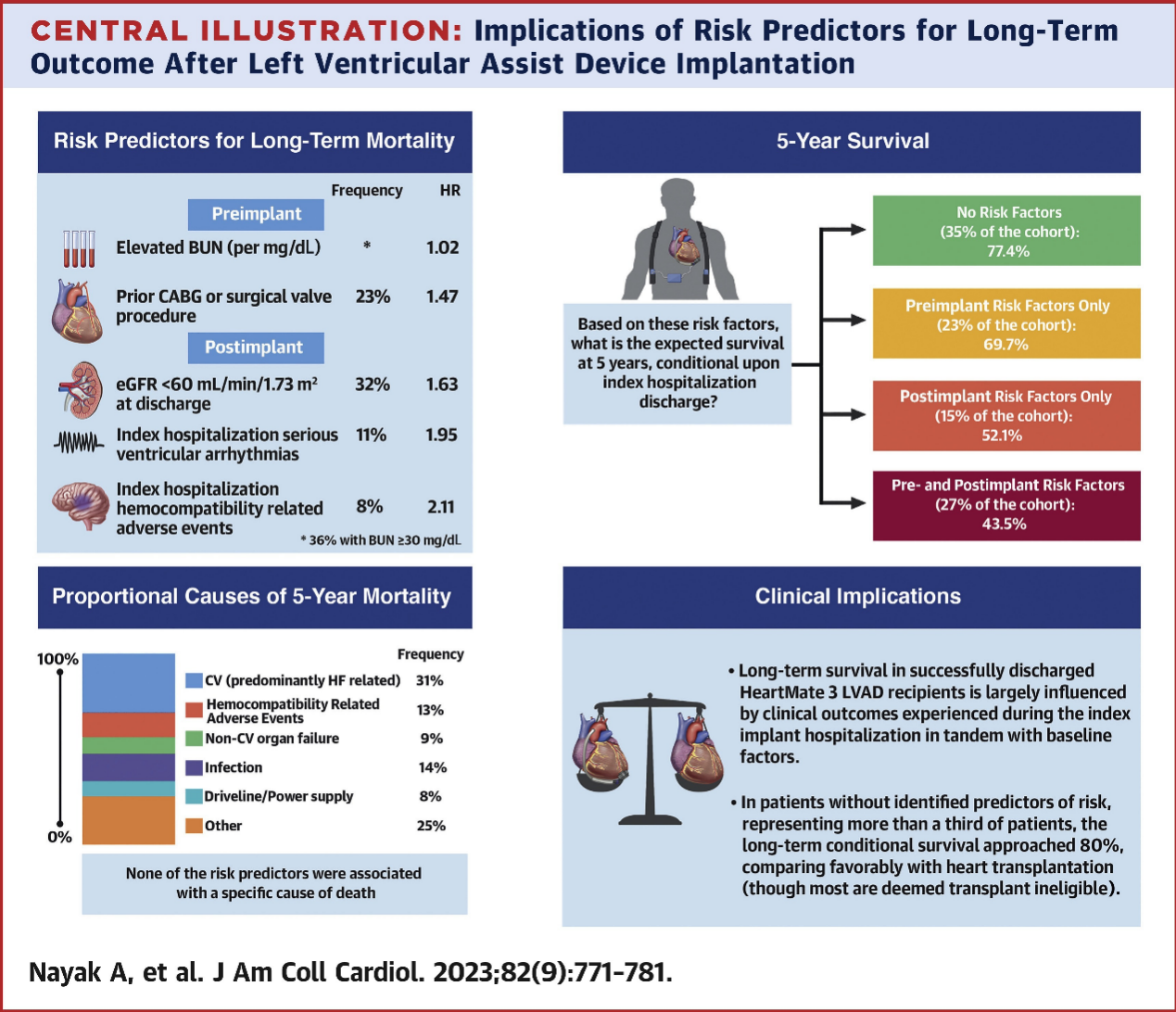
长期机械循环辅助(dMCS)
国内外机械循环辅助研究进展
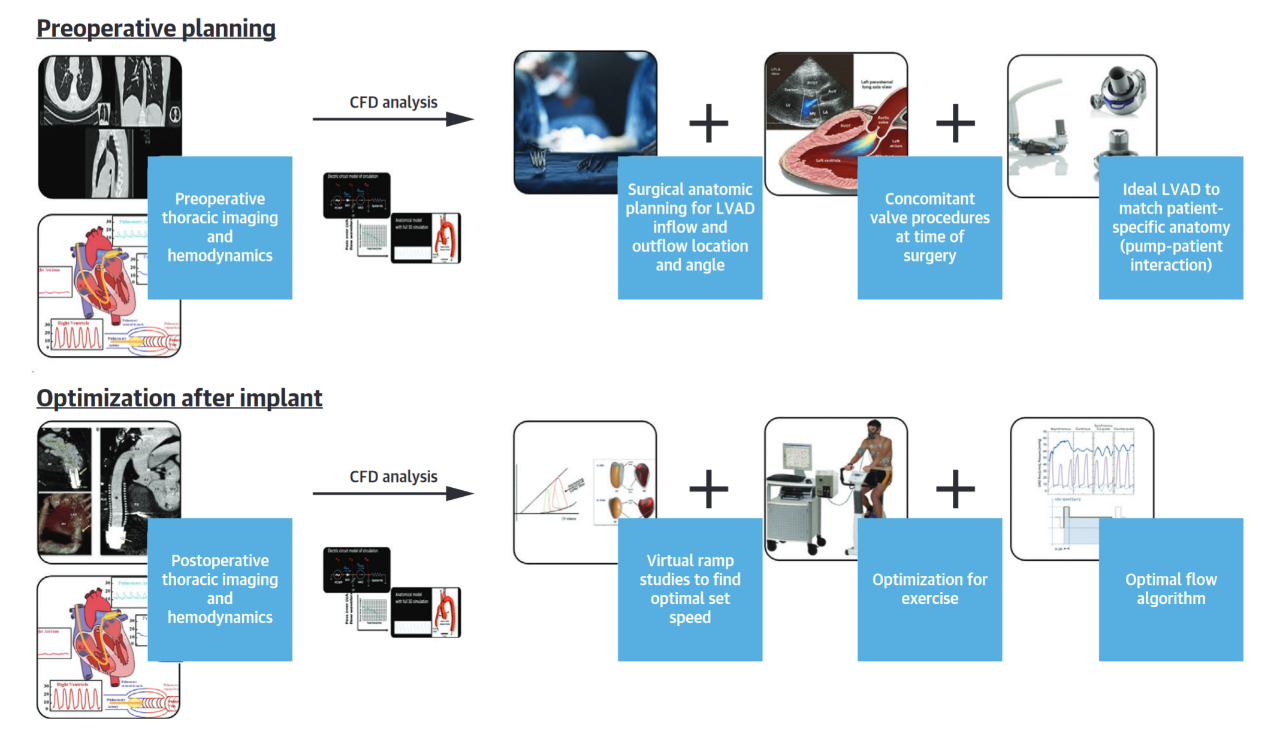
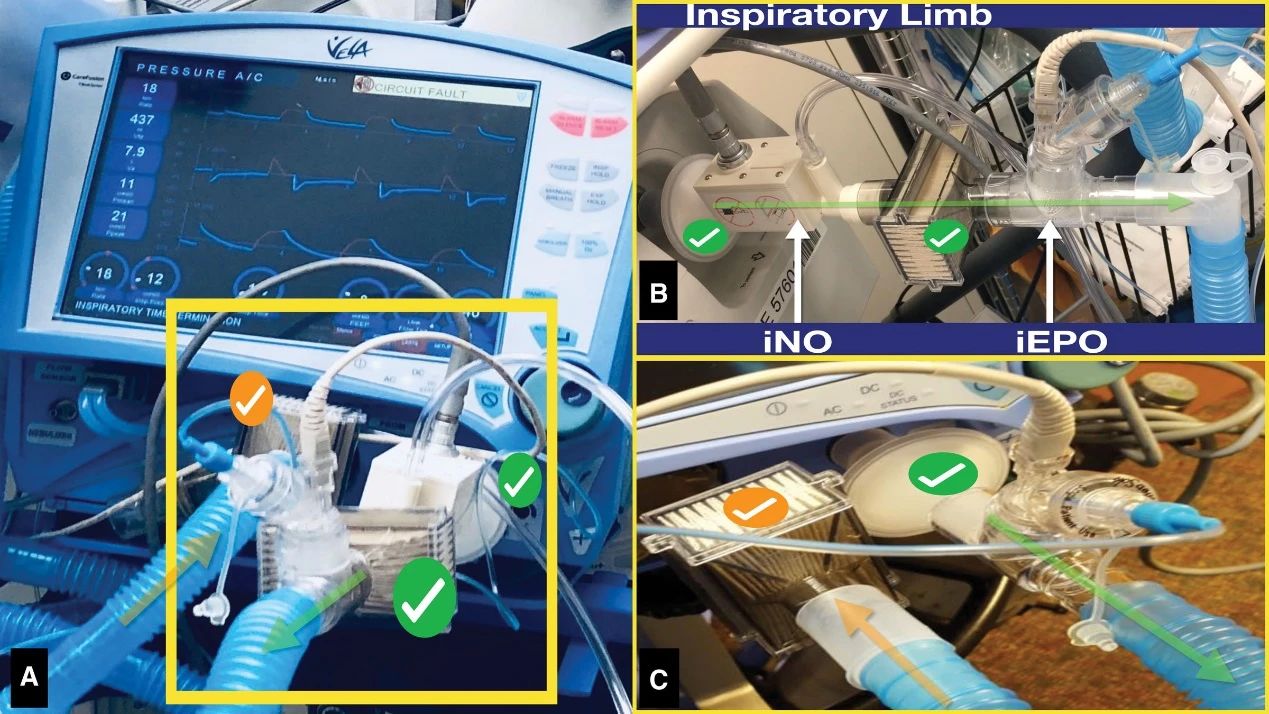
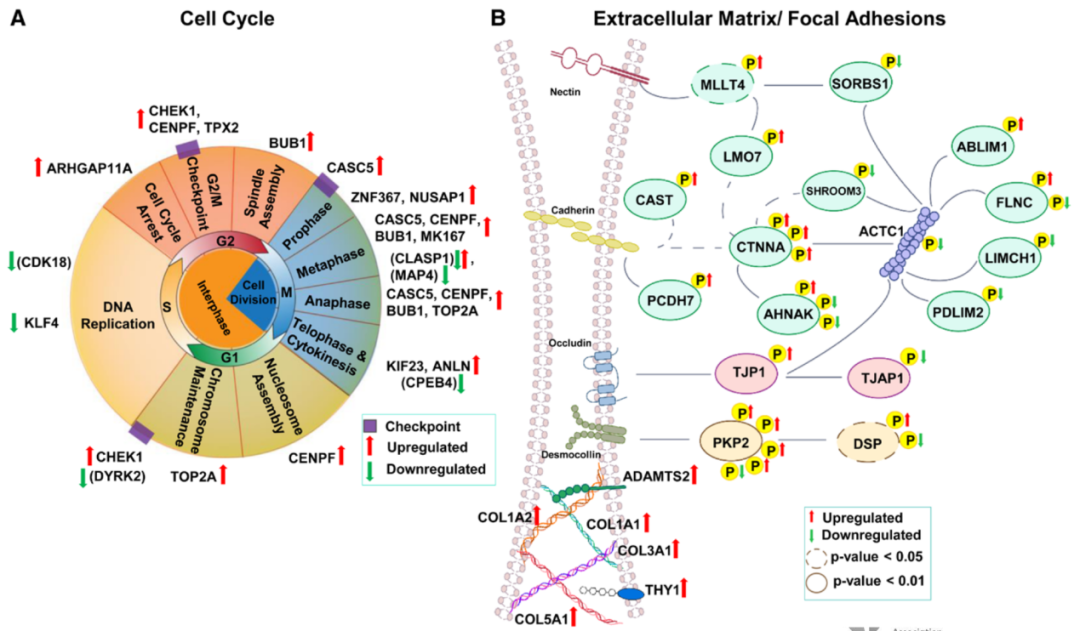
国产短中期心室辅助发展迅猛
专家简介
董念国
华中科技大学同济医学院附属协和医院
王怡轩
华中科技大学同济医学院附属协和医院


