遗传性主动脉疾病的基因组测序——400 例患者的基因突变分析
【摘要】 目的 对遗传性主动脉疾病(HAD)患者多个相关基因进行检测分型及基因突变分析。方法 依据主动脉疾病基因检测推荐指南,筛查了 2017 年以来收治的 400 例疑似 HAD 患者,对已知的 15 个 HAD 候选基因进行二代测序,然后进行 Sanger 测序验证。若二代测序结果为阴性时,如先证者临床指征明显或有家族史,则考虑大片段缺失 / 插入检测或全外显子检测,根据检测结果进行统计分析。结果 纳入的 400 例患者中,204 例(50.3%)患者共检测出 235 个可报告变异位点,主要以 FBN1 位点突变(136 个,57.9%)较为常见,其余均为其他基因的罕见突变。400 例患者中,121 例(30.25%)为(可能)致病性突变, 196 例(49.00%)为(可能良性 / 良性)或无突变,其余 83 例(20.75%)均为临床意义未明的突变。而对临床指征明显或有家族史的 13 例患者的大片段缺失 / 插入检测结果显示,其中 9 例结果为阳性。结论 基于二代测序方法有效地检测出半数患者存在基因突变,且有 30.25% 的患者可明确其基因致病性,20.75% 的患者突变基因尚待更多的循证医学数据进行验证。本研究不仅有助于临床医师早期鉴别诊断疾病类型,为患者实行个性化诊疗,而且丰富了基因谱数据,为相关基因突变的致病性判读提供循证证据。
【关键词】 遗传性主动脉疾病;基因测序;基因突变
遗传性主动脉疾病(heritable aortic disorder, HAD)是一组由致病基因变异引起的具有高度异质性及显性遗传风险的血管类疾病,多以胸主动脉瘤/夹层(thoracic aortic aneurysms/dissection, TAAD)、主动脉扩张为特征。HAD 主要分为综合征性和非综合征性两大类,综合征性 HAD 包括马方综合征(Marfan syndrome,MFS)、勒斯 - 迪茨综合征(Loeys-Dietz syndrome,LDS)、埃勒斯 - 当洛综合征(Ehlers-Danlos syndrome,EDS)、腭心面综合征(velo-cardiofacial syndrome,VCS)、动脉扭曲综合征(arterial tortuosity syndrome, ATS) 等,非综合征性 HAD 包括家族性胸主动脉瘤 / 夹 层(familial thoracic aortic aneurysm and dissection,FTAAD)、主动脉瓣二叶畸形(bicuspid aortic valve,BAV) 等。这些疾病往往存在不同程度的临床表型重合,又具有各自的异质特征。HAD 往往发病隐匿,起病急骤,误诊率高,救治率低,若不及时诊治,易发生致命性动脉瘤破裂,约40% 的 TAAD 患者存在明显的家族史。因此,早期精准鉴别诊断疾病类型对于降低 HAD 患者死亡率和提高患者生存质量具有重要意义。近年来,随着新一代测序(next generation sequencing, NGS)技术与平台的迅速发展,基因检测已成为胸主动脉疾病临床诊疗的重要手段。目前,主动脉直径大小仍然是 TAAD 患者进行外科手术干预的主要标准,但是有证据和指南表明,具有特定基因突变的患者需要在主动脉直径较小时就进行早期干预。此外,《中国单基因遗传性心血管疾病基因诊断指南》中明确指出,对于明确致病基因突变的患者, 若有意愿并在符合伦理的前提下,可通过选择性生育获得不携带该致病基因突变的后代,避免将疾病传给下一代,以减轻社会和家庭经济和精神的双重负担。因此,基因检测结果不仅可以对胸主动脉疾病进行早期的精准诊断,还对疾病的治疗策略制定、预后危险分层、遗传筛查及选择性生育等具有重要的指导作用。本研究结合 2017 年以来空军军医大学西京医院收治的 400 例疑似 HAD 患者的基因检测数据,整理家系资料,从年龄、性别、临床资料等多方面分析相关基因突变频率及致病性结论,旨在为医疗专业人员对主动脉疾病患者及其亲属的鉴别诊断和精准治疗提供指导,也为改善患者预后提供更多有价值的信息。
01 资料与方法
1.1 研究对象
本研究对 2017 年以来空军军医大学西京医院收治的 400 例疑似 HAD 患者, 依据 2014 年欧洲心脏病协会(European Society of Cardiology, ESC)《主动脉疾病诊治指南》及 2019 年《遗传性胸主动脉瘤 / 夹层基因检测及临床诊疗专家共识》进行筛查。本研究严格按照空军军医大学西京医院伦理委员会要求,在征得每位患者的知情同意后,收集患者临床资料,同时遵循赫尔辛基宣言中概述的原则。
1.2 临床资料采集
收集患者的临床资料,包括基本信息(身高、体重、年龄、性别等),既往史、手术史、家族史、临床症状及辅助检查(主要涉及心血管系统、骨骼系统、眼睛及其他),手术情况等。
1.3 血液 DNA 制备
采集患者外周血 4 ml,根据血液 DNA 试剂盒(上海百傲,中国)说明书提取 DNA,使用NANODROP 2000 检测 DNA 浓度,并通过琼脂糖凝胶电泳对提取 DNA 进行质量控制,根据测定结果进行计算,将 DNA 浓度稀释至 5 ng/μl 待用。
1.4 基因测序
根据一般二代测序流程,经过多重 PCR 扩增 - 文库制备 - 磁珠富集 - 建库 - 上机测序等过程,每 10 个样本使用 1 个 panal 芯片(赛默飞,美国),检测的基因组芯片包括已知与主动脉疾病相关的 15 个基因,包括 FBN1 、TGFBR1 、TGFBR2 、SMAD3 、TGFB2 、MYH11 、ACTA2 、SKI 、MYLK 、COL3A1 、SLC2A10 、SMAD4 、NOTCH1 、FBN2 、PRKG1 。对检测出的所有突变位点进行 Sanger 测序验证确认有无假阳性。针对有明显临床症状或者家族史的患者,若 NGS 检测结果为阴性(即15 个基因均未发现变异),则考虑进行多重连接探针扩增技术(multiplex ligation-dependent probe amplification,MLPA) 检测, 主要检测靶区域为FBN1 和TGFBR2 两个基因的全部外显子。若 MLPA 检测仍为阴性,则考虑进行全外显子组测序(whole exon sequencing,WES)。
1.5 家系筛查
根据患者检测结果,若携带临床意义未明的突变位点,对其一级亲属样本进行 Sanger 测序验证,以确认其致病性。若突变位点确定为致病性突变, 则进行整个家系筛查。
1.6 测序数据分析
使用 IonReporter 对测序的原始数据进行注释,并经系统软件进行突变分析。针对不同类型的变异选用 Human Splicing Finder、MutationTaster、SIFT 和 Polyphen 等软件再次进行分析, 参考 HGMD、UMD 和 ClinVar 等数据库及文献期刊,并结合美国医学遗传学与基因组学学会(American College of Medical Genetics and Genomics,ACMG)制定的《遗传变异分类标准与指南》判读突变位点及变异区段的致病性。
1.7 统计学分析
采用 SPSS 26.0 统计学软件进行统计学分析。计量资料经统计学分析符合正态分布者,以x±s表示,并采用 t 检验进行比较;符合偏态分布者,以M(QR)表示,并采用Mann-Whitney U 检验进行比较。计数资料采用 χ2 检验或 Fisher 确切概率法进行比较。以P<0.05>
02 结 果
2.1 临床特征分析
本组 400 例疑似 HAD 患者平均年龄为(37.0±12.4) 岁, 其中男 299 例(74.75%), 女101 例(25.25%)。基因检测结果按照突变基因致病等级顺序分类,若同时携带两类突变,则分为致病等级较高一类。其中 121 例(30.25%)检测出(可能)致病性突变,83 例(20.75%)是临床意义未明的突变,196 例(49.00%)为可能良性/ 良性或无突变;其中 96 例(24.00%)患者有猝死或 TAAD 家族史。由于临床意义未明的突变无法确定其致病性,因此本研究将携带(可能)致病性突变(A 组)与可能良性 / 良性或无突变(B 组)患者的临床特征进行比较(表 1)。
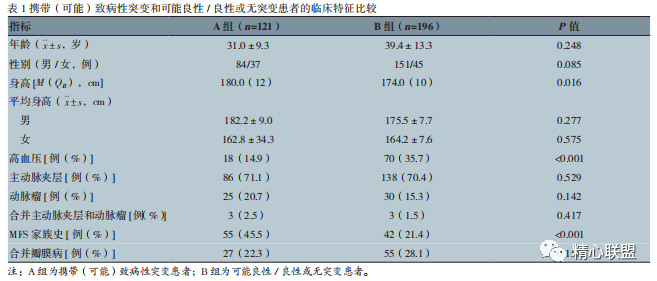
表 1 显示,A 组患者较 B 组患者年轻,但差异无统计学意义(P > 0.05)。A 组患者身高高于 B 组患者(P < 0.05)。A 组患者患高血压比例低于 B 组患者(P < 0.001), 且 A 组患者有猝死史、MFS 家族史或者主动脉瘤 / 夹层家族史的比例也高于B 组患者(P < 0.001)。而两组患者患主动脉夹层、主动脉瘤或合并主动脉夹层 / 动脉瘤及合并瓣膜病的比例比较差异无统计学意义(P > 0.05)。由此表明,无论患者是否患有主动脉夹层、主动脉瘤或合并主动脉夹层 / 动脉瘤及合并瓣膜病,都可能有遗传变异的风险。
2.2 基因变异分布特征
对 400 例疑似 HAD 患者的二代测序结果显示, 共检测出 204 例(50.3%) 患者 256 个突变位点,其中 235 个为可报告变异(即致病性 / 可能变异 + 临床意义未明变异)。根据美国医学遗传学与基因组学学会(The American College of Medical Genetics and Genomics,ACMG)和分子病理协会(The Association for Molecular Pathology,AMP) 制定的ACMG/AMP 变异分类指南,121 个突变位点(59.0%) 判读为(可能)致病性突变,114 个突变位点(55.6%) 被分类为临床意义未明变异(图 1)。
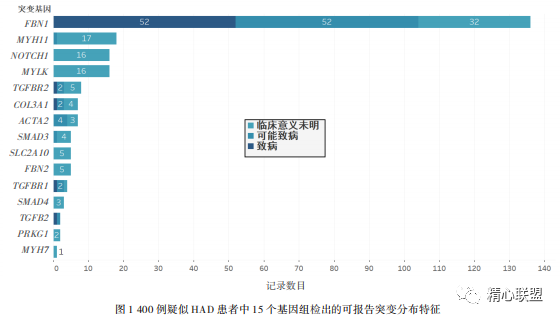
基因检测结果显示,部分患者同时携带了几种突变,可能是致病性突变、可能致病性突变、临床意义未明、可能良性 / 良性突变,故变异患者数量和变异位点数量不一致。在 235 个可报告变异中,ClinVar、HGMD 或 UMD 数据库中报告了 94 个(46.8%),141 个突变位点(53.2%)是本研究报道。此外,在所有可报告变异中,FBN1 突变占57.9%, 且在所有 FBN1 变异中,(可能)致病性突变占 76.5%,致病率最高。值得注意的是,在 14例患者中检测到TGFBR1 、TGFBR2 或TGFB2 突变, 其中 8 例是(可能)致病性突变,临床上表现为典型的 LDS。在 7 例患者中检测到可报告的 COL3A1 基因位点突变,其中有 3 例确定为(可能)致病性突变,在临床上表现为典型的 EDS。而在检测到ACTA2 突变的 7 例患者中,有 4 例判读为(可能) 致病性突变,表现为经典的家族性胸主动脉瘤。
2.3 MLPA 检测与临床表型分析
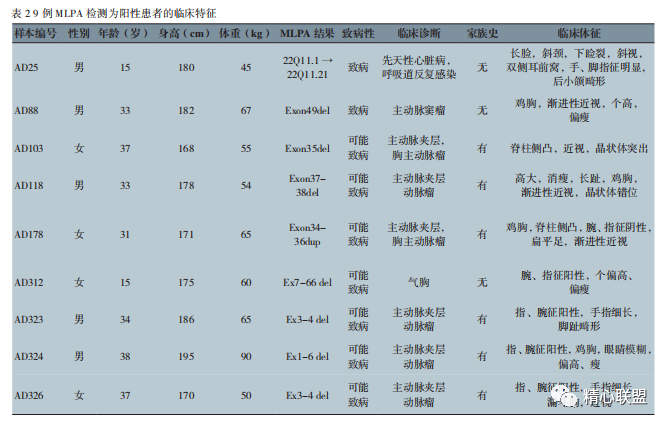
对二代测序结果为阴性且有明显家族史或者临床体征明显的 13 例患者进行了 MLPA 测序,9 例患者检测出阳性(表 2)。其中 1 例(AD25)为经典的猫眼综合征患者,其余 8 例均为编码 fibrillin-1 蛋白的部分外显子缺失或重复,表现为 MFS。这些患者年龄为 15~38 岁,均较为年轻,无性别差异, 身高偏高,体型偏瘦,临床指征较为明显,大部分合并猝死等家族史。
03 讨 论
随着分子生物学技术的不断发展及人类基因组计划的开展,疾病的分子诊断作为临床上一种独特的临床诊断方法已得到广泛的应用。目前,临床上开展较多的是对疾病相关的已知致病基因进行 NGS 筛查,检测患者是否存在突变并确定其致病性。本研究针对 HAD 相关的 15 个基因,对 400 例疑似HAD 患者进行了 NGS 检测。本研究在 204 例患者(50.3%)中发现了 235 个可报告突变位点,其中141 个变异位点是本研究检测到的,这不仅丰富了人类基因突变谱,对临床上鉴别诊断和个性化治疗具有极大的帮助。根据ACMG/AMP 变异分类指南, 235 个可报告变异中有59.0% 为(可能)致病性突变, 因此,通过基因检测为临床医师寻找疾病病因提供了依据。
本研究中,患者平均年龄为(37.0±12.4)岁, 低于国人主动脉夹层注册中心(sino-RAD)的急性主动脉夹层患者的(51.8±11.4)岁,男性患者占 74.75%,与文献报道相近。同时,本研究表明,携带(可能)致病性突变患者身高比可能良性 / 良性或无突变患者更高,而高血压却更常见于可能良性 / 良性或无突变患者。由于高血压往往是非遗传性主动脉疾病的主要易感因素,而携带(可能) 致病性突变患者呈现出更多的家族聚集现象,这些均与 MFS 等 HAD 的临床特征相符合。总之,两组患者临床表型差异较大,反映出两组不同的病理生理过程。
HAD 可发生于 MFS、LDS、EDS、FTAAD 等多种疾病。本研究纳入的 400 例疑似 HAD 患者中 14 例检出 LDS 相关基因TGFBR1 、TGFBR2 或 TGFB2 的突变,其中 8 例患者为(可能)致病性变异体, 这类疾病往往发病年龄更早 [(27.9±12.3)岁 ], 心血管系统和骨骼系统与 MFS 有着相似表现,也表现出一些异质性,如眼距过宽、悬雍垂 / 腭裂、颅缝早闭、动脉扭曲等,而且合并主动脉瘤 / 夹层临床进展更为迅猛。同样,在 7 例患者中检测到EDS 相关基因COL3A1 位点突变,其中有 3 例为(可能)致病性变异体,此类疾病往往会引发严重的并发症,如胃肠穿孔及妊娠子宫破裂,由于其临床表现为皮肤弹力过度、皮肤和血管脆性增加、伤口难以愈合且易形成萎缩性瘢痕、全身性的关节活动过度等,这与临床观察一致。此外,本研究与之前的报道类似, FBN1 变异例数最多,致病率最高,患者对此病认知度最高,发病率为1:3000~1:5000,可表现为多个器官系统受累,主要涉及心血管、骨骼和眼部,若无早期识别诊断,极易发生猝死等灾难性危害。
由于二代测序技术存在局限性,对大片段基因的缺失 / 插入无法测得,在高达 7% 的 MFS 患者中存在这种情况。故 2010 年修订版 Ghent 诊断标准推荐采用 MLPA 来检测 MFA 患者是否存在大基因片段的缺失 / 插入。本研究对 NGS 检测为阴性且有家族史或者临床体征明显的 13 例患者进行了 MLPA 检测,其中 9 例检测出阳性,7 例为本研究报道。有意义的是,本研究发现了 1 例猫眼综合征患者,其额外标记染色体 22q11.1-q22.2 重复了1.76 Mb,但该病例与其他病例不同的是,患者没有明显的精神残疾,身高比同龄人高。以上证明了, 在多系统受累且 NGS 测序结果为阴性的患者中筛查基因大片段缺失 / 插入是有效且实用的。
综上, 本研究通过 NGS 和 MLPA 技术对 2017 年以来空军军医大学西京医院就诊的 400 例疑似HAD 患者进行了 HAD 相关基因的检测,为临床上精准的个性化治疗、遗传阻断提供了科学依据,同时也丰富了基因组学数据库。
专家简介

段维勋 教授
段维勋,男,1977年12月生,副教授、博士研究生导师,现任空军军医大学第一附属医院心血管外科实验室主任。先后担任中国医师学会分会副秘书长、国家心血管病血管外科专业委员会委员、陕西省生理科学会理事。以第一/通信作者发表 SCI 论文40余篇,9篇IF>10,获国家科技进步二等奖和中华医学一等奖,获陕西省青年科技奖和陕西省高层人才资助,以第一完成人获国家发明专利2项、实用新型专利3项。近五年共主持国家重点研发计划课题1项,国家自然科学基金3项,陕西省重点研发计划2项,共计经费500余万。主要研究方向为大血管疾病及成人心脏病外科治疗等临床和基础研究工作,担任外科大血管外科治疗组组长,负责建立主动脉夹层动脉瘤“绿色通道”,开展主动脉夹层杂交手术、术中三分支支架技术、术中弓部支架开窗术等临床新技术。
作者单位:710032 西安市 空军军医大学西京医院
1.心血管外科,2. 检验科
*通信作者:段维勋 Email:duanweixun@126.com DOI:10.16563/j.cnki.1671-6272.2022.06.001
转载自 精心联盟


