
2023年01月13日,据Vascularnews报道,欧洲血管外科学会(ESVS)腹主动脉瘤指南编委会发布了,关于Nellix血管内动脉瘤封闭系统(EVAS)修复肾下腹主动脉瘤(AAA)患者的监测和管理建议。ESVS建议对所有植入Nellix设备的患者进行识别,并适当加强管理及监测。如果发现器械故障,则应考虑在适合手术病人的早期选择器械植入。该建议由剑桥大学医学院Jon Boyle教授等人撰写,已于2023年01月06日发表在《欧洲血管和腔内外科杂志》(EJVES)上。

Boyle及其同事指出,截至2022年12月7日,根据 PubMed的文献检索结果,他们对接受EVAS治疗的AAA患者发生严重主动脉相关不良事件的风险进行了系统评价。欧洲血管外科学会(ESVS)腹主动脉瘤指南编委会同意了欧洲心脏病学会(ESC)分级系统的建议。
作者写道:“EVAS具有很高的晚期移植物迁移发生率,导致近端1型内漏伴有破裂风险,需要与器械植入物进行开放性转换。”作者在文中还详细介绍了他们在系统评价中的关键发现。他们补充说:“选择性移植报道的死亡率在0%到14%之间变化,而急性破裂转换的预后则非常差,死亡率为67%到75%。”
作者介绍了ESVS指南每五年左右更新一次,此外还发布了ESVS重点更新内容,以公布出在完整指南发布之前出现的一些颇为重要的新数据,这些数据对患者的安全或管理及决策都有着重要的影响”。
去年5月,由于 Nellix EVAS系统植入后,动脉瘤囊扩大导致内漏发生率较高,Endologix公司已终止了该系统的生产。然而,指南委员会认识到,对于已经使用 EVAS装置进行AAA修复的患者,并没有明确的监测和管理指导。正是由于这个原因,欧洲血管外科学会(ESVS)腹主动脉瘤指南编委会发起了一项关于此主题的系统评价。他们在新论文中写道: “目前积累的实践表明,接受EVAS治疗的AAA患者可能存在较高的不良事件发生风险,这证明了对已经接受EVAS治疗的患者进行监测及管理的最新指导是合理的。”
欧洲血管外科学会(ESVS)腹主动脉瘤指南编委会,在评论其发布的时间时指出:“决定在2024年全面更新指南发布之前发布此次建议是非常重要的,以强调EVAS失败的问题来促进患者的安全,并鼓励临床医生识别所有已植入Nellix设备的患者”。
关于Nellix®
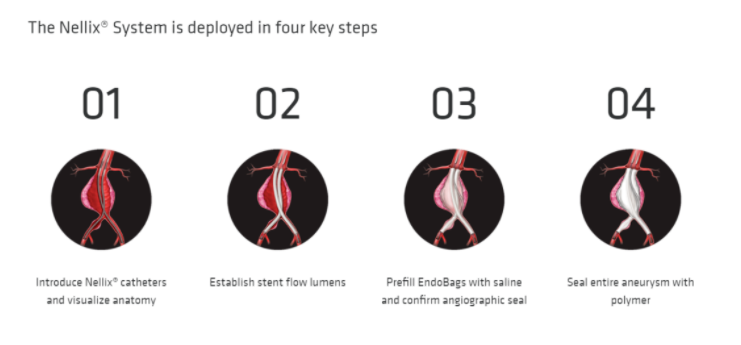
Nellix是第一个也是唯一一个通过密封整个动脉瘤囊来治疗腹腔动脉瘤的系统,该系统包括输送系统、植入物及聚合物三部分组成。Nellix®是一种治疗AAA的新方法,涉及双侧支架和生物稳定及生物相容的聚合物,注入符合要求的EndoBags,密封整个动脉瘤。Nellix植入物可在CT和/或超声下进行成像,随着时间的推移,Nellix植入物的特征很容易被看到,以便进行有效的长期监测。
关于Endologix
Endologix是一家总部设在美国加州的全球性医疗器械公司,致力于通过为血管疾病的介入治疗提供创新疗法来改善患者的生活。Endologix公司的治疗组合包括各种处于不同开发阶段的产品,这些产品旨在治疗目前在临床上尚未满足需求的疾病。这些产品旨在治疗从腹主动脉瘤到下肢外周血管疾病的广泛的血管疾病。通过对产品设计、制造和培训的一丝不苟,以及所有行业领先的临床证据的支持,将取得优异的临床结果。Endologix的腹主动脉瘤(AAA)产品建立在两个平台,传统的微创血管内动脉瘤修复术(EVAR)和血管内动脉瘤封堵术(EVAS),后者是研究性产品。Endologix目前上市EVAR产品包括AFX®2设备和ALTO®腹部支架移植系统。2020年10月1日,Endologix成为一家私人公司,由Deerfield Management(Deerfield是一家投资管理公司,致力于通过投资、信息和慈善事业推进医疗保健)全资拥有。该公司在尔湾和圣罗莎设有办事处和生产基地。


